问题补充:
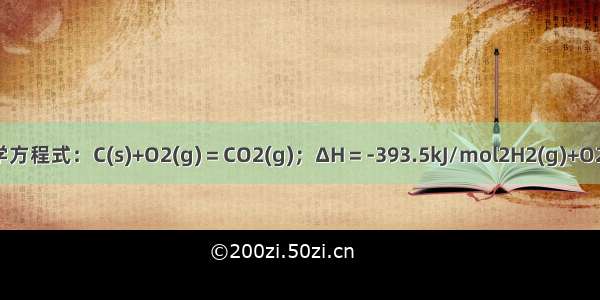
已知下列热化学方程式:
①CH4(g)+2O2(g)==CO2(g)+2H2O(l)△H=-889.5kJ/mol
②2C2H6(g)+7O2(g)==4CO2(g)+6H2O(l)△H=-3116.7kJ/mol
③C2H4(g)+3O2(g)==2CO2(g)+2H2O(l)△H=-1409.6kJ/mol
④2C2H2(g)+5O2(g)==4CO2(g)+2H2O(l)△H=-2596.7kJ/mol
⑤C3H8(g)+5O2(g)==3CO2(g)+4H2O(l)△H=-2217.8kJ/mol现有由上述五种烃中的两种组合成的混合气体2mol,经充分燃烧后放出3037.6kJ热量,则下列哪些组合是不可能的A.C2H4和C2H6B.C2H2和C3H8C.C2H6和C3H8D.C2H6和CH4
答案:
C解析混合气体2mol,经充分燃烧后放出3037.6kJ热量,则平均1mol混合气体完全燃烧放出的热量是1518.8kJ。根据热化学方程式可知,1mol上述5中烃完全燃烧放出的热量分别是889.5kJ、1558.35kJ、1409.6kJ、1298.35kJ、2217.8kJ,所以根据平均值原理可知,选项C是不可能的,