问题补充:
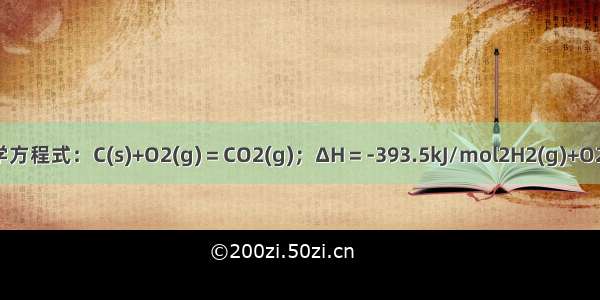
已知下列两个热化学方程式:2CO(g) + O2(g) = 2CO2(g)△H =- 586.7 kJ/mol2H2(g) + O2(g) = 2H2O(l) △H =-571.6 kJ/mol,实验测得:CO与H2的混合气体5.8g,完全燃烧时,放出的热量为87.25KJ,则混合气体中CO和H2的体积比为A.1 :1B.2 :1C.2 :3D.1 :3
答案:
B解析试题分析:设CO xmol,H2 ymol,则 28x+2y=5.8解得 x=0.2y=0.1,所以体积比为2:1。